初中化学人教版9年级上下全册知识点 - 初中化学方程式汇总
初中化学方程式汇总
一、 氧气的性质:
■单质与氧气的反应:
镁在空气中燃烧:2mg o2 2mgo
2mgo
铁在氧气中燃烧:3fe 2o2 fe3o4 (注意生成物不是fe2o3)
fe3o4 (注意生成物不是fe2o3)
铜在空气中受热:2cu o2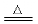 2cuo
2cuo
铝在空气中燃烧:4al 3o2  2al2o3 (注意不要将al2o3写成alo)
2al2o3 (注意不要将al2o3写成alo)
氢气中空气中燃烧:2h2 o2 2h2o
2h2o
红磷在空气中燃烧(研究空气组成的实验):4p 5o2 2p2o5
2p2o5
硫粉在空气中燃烧:s o2 so2
so2
碳在氧气中充分燃烧:c o2 co2
co2
碳在氧气中不充分燃烧:2c o2 2co
2co
■化合物与o2的反应:
一氧化碳在氧气中燃烧:2co o2 2co2
2co2
甲烷在空气中燃烧:ch4 2o2 co2 2h2o
co2 2h2o
酒精在空气中燃烧:c2h5oh 3o2 2co2 3h2o
2co2 3h2o
■o2的来源:
玻义耳研究空气的成分实验 2hgo hg o2 ↑
hg o2 ↑
原理1加热高锰酸钾:2kmno4 k2mno4 mno2 o2↑
k2mno4 mno2 o2↑
原理2氯酸钾制取氧气:2kclo3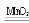 2kcl 3o2↑
2kcl 3o2↑
原理3过氧化氢在二氧化锰作催化剂条件下分解反应:2h2o2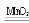 2h2o o2 ↑
2h2o o2 ↑
二、自然界中的水:
水在直流电的作用下分解(研究水的组成实验):2h2o 2h2↑ o2 ↑
2h2↑ o2 ↑
生石灰溶于水:cao h2o == ca(oh)2
二氧化碳可溶于水:h2o co2==h2co3
三、质量守恒定律:
镁在空气中燃烧:2mg o2 2mgo
2mgo
铁和硫酸铜溶液反应:fe cuso4 === feso4 cu
氢气还原氧化铜:h2 cuo  cu h2o
cu h2o
四、碳和碳的氧化物:
■碳的化学性质
碳在氧气中充分燃烧:c o2 co2
co2
木炭还原氧化铜:c 2cuo  2cu co2↑
2cu co2↑
焦炭还原氧化铁:3c 2fe2o3 4fe 3co2↑
4fe 3co2↑
■煤炉中发生的三个反应:(几个化合反应)
底层:c o2 co2
co2
煤炉的中层:co2 c  2co
2co
煤炉的上部蓝色火焰的产生:2co o2 2co2
2co2
■二氧化碳的制法与性质:
大理石与稀盐酸反应(实验室制二氧化碳):caco3 2hcl == cacl2 h2o co2↑
碳酸不稳定而分解:h2co3 == h2o co2↑
二氧化碳可溶于水:h2o co2== h2co3
高温煅烧石灰石(工业制二氧化碳):caco3 cao co2↑
cao co2↑
石灰水与二氧化碳反应(鉴别二氧化碳):ca(oh)2 co2 == caco3 ↓ h2o
■一氧化碳的性质:
一氧化碳还原氧化铜:co cuo  cu co2 (注意条件不是高温)
cu co2 (注意条件不是高温)
一氧化碳的可燃性:2co o2 2co2
2co2
■其它反应:
碳酸钠与稀盐酸反应(灭火器的原理):
na2co3 2hcl == 2nacl h2o co2↑ (注意不要将na2co3写成naco3)
五、燃料及其利用:
甲烷在空气中燃烧:ch4 2o2 co2 2h2o
co2 2h2o
酒精在空气中燃烧:c2h5oh 3o2 2co2 3h2o
2co2 3h2o
氢气中空气中燃烧:2h2 o2 2h2o
2h2o
六、金属
■金属与o2反应:
镁在空气中燃烧:2mg o2 2mgo(注意不要将mgo写成mgo2)
2mgo(注意不要将mgo写成mgo2)
铁在氧气中燃烧:3fe 2o2 fe3o4(注意不要将fe3o4写成fe2o3)
fe3o4(注意不要将fe3o4写成fe2o3)
铜在空气中受热:2cu o2 2cuo
2cuo
铝在空气中形成氧化膜:4al 3o2 = 2al2o3
■金属单质 酸 -------- 盐 h2↑ (置换反应)
锌和稀硫酸zn h2so4 = znso4 h2↑
铁和稀硫酸fe h2so4 = feso4 h2↑
镁和稀硫酸mg h2so4 = mgso4 h2↑
铝和稀硫酸2al 3h2so4 = al2(so4)3 3 h2↑
锌和稀盐酸zn 2hcl == zncl2 h2↑
铁和稀盐酸fe 2hcl == fecl2 h2↑(注意不要将fecl2写成fecl3)
镁和稀盐酸mg 2hcl == mgcl2 h2↑
铝和稀盐酸2al 6hcl == 2alcl3 3 h2↑
■金属单质 盐(溶液) ------- 新金属 新盐
铁和硫酸铜溶液反应:fe cuso4 == feso4 cu
锌和硫酸铜溶液反应:zn cuso4 ==znso4 cu
铜和硝酸汞溶液反应:cu hg(no3)2 == cu(no3)2 hg
■金属铁的治炼原理:3co fe2o3 2fe 3co2
2fe 3co2
七、酸、碱、盐
1、酸的化学性质
■酸 金属 → 盐 氢气(见上)
■酸 金属氧化物→ 盐 水
稀盐酸除铁锈的反应:fe2o3 6hcl ==2fecl3 3h2o
稀硫酸除铁锈的反应:fe2o3 3h2so4 == fe2(so4)3 3h2o
氧化铜和稀盐酸反应:cuo 2hcl ==cucl2 h2o
氧化铜和稀硫酸反应:cuo h2so4 == cuso4 h2o
■酸 碱→盐 水(中和反应)
盐酸和烧碱起反应:hcl naoh == nacl h2o
盐酸和氢氧化钙反应:2hcl ca(oh)2 == cacl2 2h2o
氢氧化铝药物治疗胃酸过多:3hcl al(oh)3 == alcl3 3h2o
硫酸和烧碱反应:h2so4 2naoh == na2so4 2h2o
■酸 盐 →新酸 新盐
大理石与稀盐酸反应:caco3 2hcl == cacl2 h2o co2↑
碳酸钠与稀盐酸反应: na2co3 2hcl == 2nacl h2o co2↑
碳酸氢钠与稀盐酸反应:nahco3 hcl== nacl h2o co2↑
硫酸和氯化钡溶液反应:h2so4 bacl2 == baso4 ↓ 2hcl
2、碱的化学性质
■ 碱 非金属氧化物 → 盐 水
苛性钠暴露在空气中变质:2naoh co2 == na2co3 h2o
苛性钠吸收二氧化硫气体:2naoh so2 == na2so3 h2o
苛性钠吸收三氧化硫气体:2naoh so3 == na2so4 h2o
消石灰放在空气中变质:ca(oh)2 co2 == caco3 ↓ h2o
消石灰吸收二氧化硫:ca(oh)2 so2 == caso3 ↓ h2o
■碱 酸→ 盐 水(中和反应,方程式酸 碱的反应)
■碱 盐 → 另一种碱 另一种盐
氢氧化钙与碳酸钠:ca(oh)2 na2co3 == caco3↓ 2naoh
3、盐的化学性质
■盐(溶液) 金属单质→新金属 新盐
铁和硫酸铜溶液反应:fe cuso4 == feso4 cu
■盐 酸→新酸 新盐
碳酸钠与稀盐酸反应: na2co3 2hcl == 2nacl h2o co2↑
碳酸氢钠与稀盐酸反应:nahco3 hcl== nacl h2o co2↑
■盐 碱 →新碱 新盐
氢氧化钙与碳酸钠:ca(oh)2 na2co3 == caco3↓ 2naoh
■盐 盐 → 两种新盐
氯化钠溶液和硝酸银溶液:nacl agno3 == agcl↓ nano3
硫酸钠和氯化钡:na2so4 bacl2 == baso4↓ 2nacl
注意:碱与盐、盐与盐的反应,生成物要有h2o、↓、↑且反应物必须可溶于水。
扫描二维码推送至手机访问。
特别声明:
本站属于公益性网站,纯粹个人原因(陪孩子学习便于查询和教授),网站部分内容收集于网络,仅供学生和老师参考、交流使用,请勿用作其他商业收费用途。
如果网站内容能给你带来提升,那便是我经营此网站的初衷。网站相关内容如有问题,请及时提出,我在此谢谢!
本站尊重原创并对原创者的文章表示肯定和感谢,如有侵权请联系删除!针对本站原创内容,本站也欢迎转载,如需转载请注明出处。